熱力学でつまづくポイントの一つに「自然な変数」があります。
例えば、内部エネルギーの「自然な変数」はエントロピー$S$と体積$V$ですが、皆さんは内部エネルギーがこの変数の組み合わせでないと表せないと勘違いしていませんか?もちろん、実際には内部エネルギーは温度$T$と体積$V$の組み合わせでも表すことができます。
では、自然な変数の組み合わせでないとなにが問題なのでしょうか?このページでは、内部エネルギーとエンタルピーを自然な変数の組み合わせで表すメリットを具体的な数値を使って考えていきます。
内部エネルギーUの自然な変数はTとVではありません
内部エネルギー$U$でもっともイメージしやすいのは温度$T$と体積$V$ごとの内部エネルギー$U(T,V)$ではないでしょうか?

複数の温度$T$、体積$V$ごとにMDを行って、内部エネルギーの結果を$T$、$V$ごとに並べたら$U(T,V)$になるよ。

飛び飛びな値の集まりとして$U(T,V)$が得られるんだね。
MDからは計算条件で与えた温度$T$、体積$V$での内部エネルギー$U$しか得られませんが、複数の温度$T$、体積$V$ごとにMDを行うと次のように$U(T,V)$が得られます。
| 内部エネルギー$U(T,V)$ | 体積$V$ | ||||
| 3000 | 3100 | ~ | 4000 | ||
| 温度$T$ | 0.90 | 976 | 988 | 1067 | |
| 0.91 | 993 | 1004 | 1084 | ||
| ~ | |||||
| 1.10 | 1305 | 1317 | 1387 | ||

さて、この$U(T,V)$について考えていきましょう。
残念ながら、$U(T,V)$は自然な変数の組み合わせではありません。例えば、体積$V=3500$の時の温度$T$に対する傾き($1644.8$)は熱力学的によくわからない値になっています。
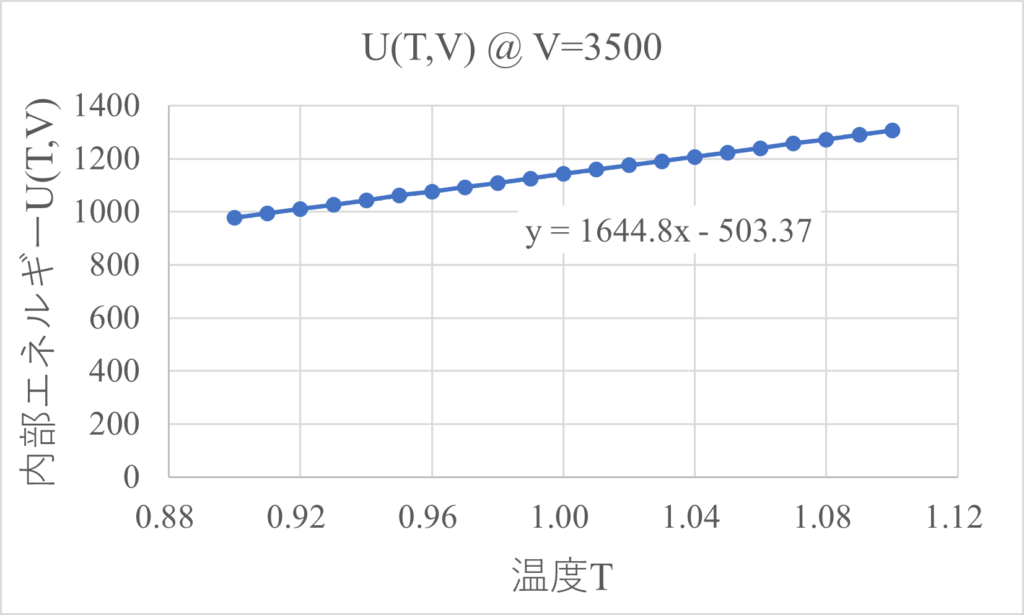

微分はできるけど、係数が意味があまりないものになっているんだね。

では次に、$U(S,V)$へ内部エネルギーの変数を変えていきましょう。
内部エネルギーUの変数をSとVに変換しよう
MDから得られている$U(T,V)$と$S(T,V)$を使うことで$U(S,V)$を作ることができます。

$S(T,V)$は熱力学第一法則使って次のように得ることができます。
| エントロピー$S(T,V)$ | 体積$V$ | ||||
| 3000 | 3100 | ~ | 4000 | ||
| 温度$T$ | 0.90 | 0.0(基準) | 65.1 | 526 | |
| 0.91 | 18.8 | 83.1 | 546 | ||
| ~ | |||||
| 1.10 | 330 | 393 | 841 | ||


$U=U(S,V)$は$U=U(T,V)$と$S=S(T,V)$からどうやって作るの?

例えば、$V=3000$における$(S,U)=(0,976),(330,1305)$の2点だけからでも$U=0.99S+976$と、$U$の$S$依存性がわかるよ。

これを$V$ごとに行うと$U(S,V)$が得られるんだね。
いま、$V$、$T$ごとの$U(T,V)$と$S(T,V)$の表から、$V$の値ごとに内部エネルギー$U$とエントロピー$S$の関係性を調べることで次のように$U=U(S,V)$を得ることができます。
| 内部エネルギー$U(S,V)$ | 体積$V$ | ||||
| 3000 | 3100 | ~ | 4000 | ||
| エントロピー$S$ | 0 | 971 | 918 | 523 | |
| 50 | 1021 | 968 | 574 | ||
| ~ | |||||
| 750 | 1718 | 1668 | 1289 | ||
この$U(S,V)$について、エントロピー$S$と体積$V$が内部エネルギー$U$の自然な変数になっていることを確認しましょう。
$\frac{\partial{U(S,V)}}{\partial{S}}=T$を確認
$V=3500$の時、$U(S,V)$のエントロピー微分$\frac{\partial{U(S,V)}}{\partial{S}}$は$1.0$となり、これは温度$T$と同じであるため、$\frac{\partial{U(S,V)}}{\partial{S}}=T$が成り立っています。
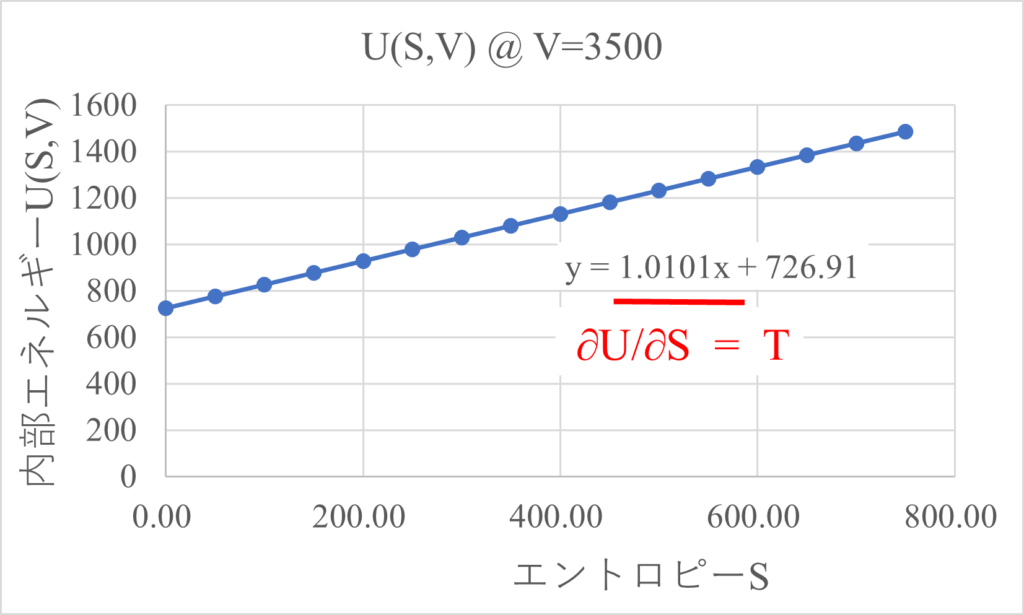
$\frac{\partial{U(S,V)}}{\partial{V}}=-P$を確認
$S=0$の時、$U(S,V)$の体積微分$\frac{\partial{U(S,V)}}{\partial{V}}$は$-0.43$となり、これは圧力$P$を負の値にしたものであるため、$\frac{\partial{U(S,V)}}{\partial{V}}=-P$が成り立っています。
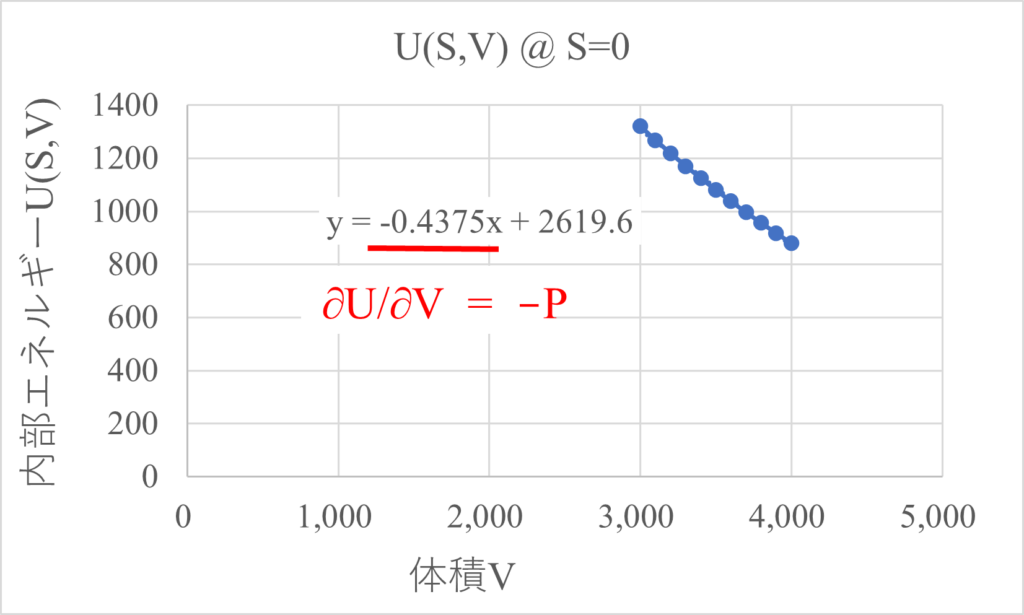
$U(S,V)$まとめ
以上から、$U(T,V)$は自然な変数の組み合わせになっていませんでしたが、$U(S,V)$は自然な変数の組み合わせになっていることがわかるかと思います。

でも、もともと$S$を$\text{d}S=\frac{1}{T}\text{d}U+\frac{P}{T}\text{d}V$から作ったから、$U(S,V)$が自然な組になるのは当然じゃない?

たしかに、その通りだね。じゃあ、次はエンタルピー$H$の自然な変数にチャレンジしてみよう。
定義を使ってエンタルピーHを求めよう
内部エネルギー$U(S,V)$が自然な変数になることは、エントロピー$S$を$\text{d}S=\frac{1}{T}\text{d}U+\frac{P}{T}\text{d}V$から作っているので、当然といえば当然です。
そこで、次は少し難易度を上げて、エンタルピー$H=U+PV$の自然な変数を調べてみましょう。

$U(S,V)$と$P(S,V)$を使って、エンタルピー$H=U+PV$を求めましょう。
エンタルピー$H$は$H=U+PV$で得ることができますが、変数に注意しましょう。MDから直接得られる圧力$P$は$P(T,V)$の形ですが、$U(S,V)$を利用する場合、圧力$P$の変数も$P(S,V)$に合わせたものを利用する必要があります。

$P(S,V)$は$U(S,V)$と同じように、MDから得られる$P(T,V)$と$S(T,V)$の依存性を調べると得ることができるね。
| エンタルピー$H(S,V)$ | 体積$V$ | ||||
| 3000 | 3100 | ~ | 4000 | ||
| エントロピー$S$ | 0 | 2399 | 2250 | 1240 | |
| 50 | 2504 | 2354 | 1341 | ||
| ~ | |||||
| 750 | 3972 | 3810 | 2753 | ||
当然ですが、この$H(S,V)$は変数が$S$と$V$のため、偏微分が熱力学量になっていません。例えば、$S=0$における$H(S,V)$の体積$V$依存性は$\frac{\partial{H(S,V)}}{\partial{V}}=-1.14$と熱力学量になっていません。
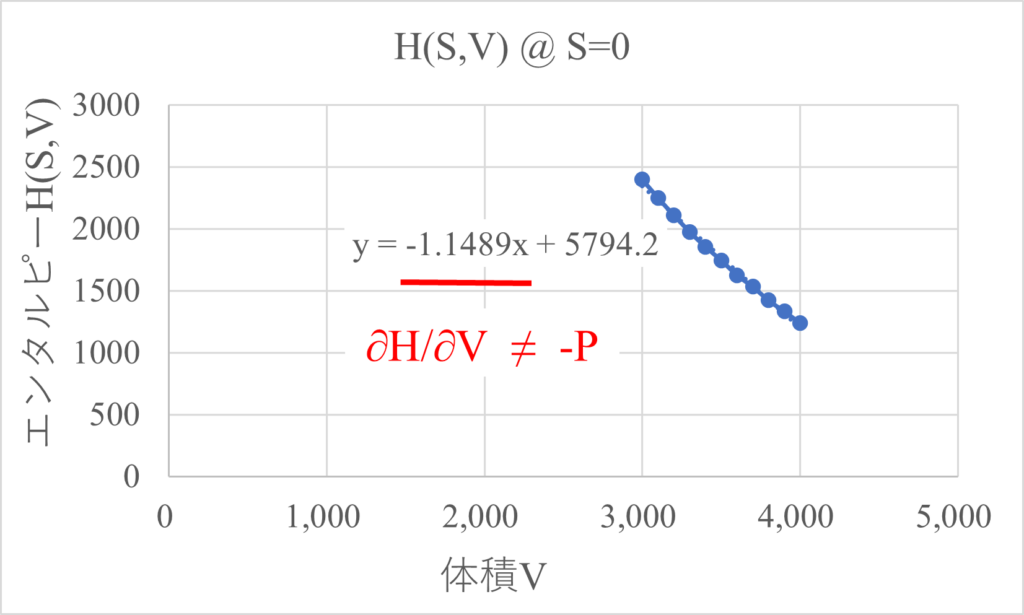

$\frac{\partial{U(S,V)}}{\partial{V}}$は$-P$になっていたのに、$H=U+PV$の微分は$-P$にならないんだね。

その代わりに$V$が自然な変数になります。早速変数を変えていきましょう。
エンタルピーHの変数をSとPに変換しよう

さて、$H(S,V)$から$H(S,P)$を作る方法わかりますか?

$P(S,V)$があれば、$V$の値ごとの$H$の$P$依存性を調べると$H(S,P)$が得られるね。
$H(S,P)$ですが、内部エネルギー$U(T,V)$から$U(S,V)$を作った時と同じように、$H(S,V)$と$P(S,V)$の関係性を調べることで$H(S,P)$の表を得ることができます。
| エンタルピー$H(S,P)$ | 圧力$P$ | ||||
| 0.2 | 0.3 | ~ | 0.7 | ||
| エントロピー$S$ | 0 | 1363 | 1753 | 3315 | |
| 50 | 1414 | 1798 | 3335 | ||
| ~ | |||||
| 750 | 2264 | 2581 | 3847 | ||
この$H(S,P)$について、エントロピー$S$と圧力$P$がエンタルピー$H$の自然な変数になっていることを確認しましょう。
$\frac{\partial{H(S,P)}}{\partial{S}}=T$を確認
$P=0.4$の時、$H(S,P)$のエントロピー微分$\frac{\partial{H(S,P)}}{\partial{S}}$は$1.0$となり、これは温度$T$と同じであるため、$\frac{\partial{H(S,P)}}{\partial{S}}=T$が成り立っています。
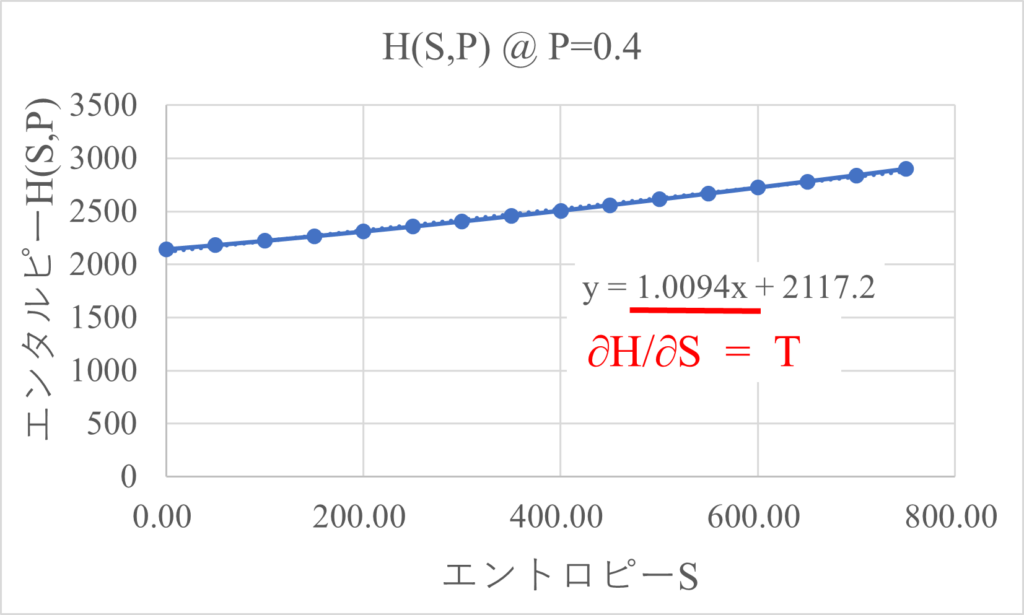
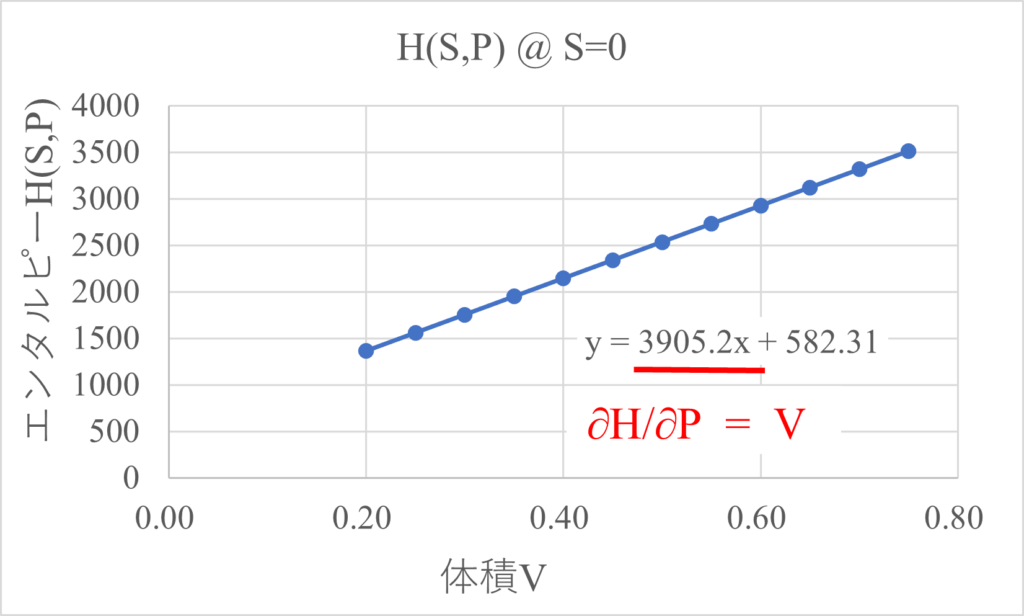
$\frac{\partial{H(S,P)}}{\partial{P}}=V$を確認
$S=0$の時、$H(S,V)$の圧力微分$\frac{\partial{H(S,P)}}{\partial{V}}$は$3905$となり、これは体積$V$と同じであるため、$\frac{\partial{H(S,P)}}{\partial{P}}=V$が成り立っています。
$H(S,P)$まとめ
以上から、$H(S,V)$は自然な変数の組み合わせになっていませんでしたが、$H(S,P)$は自然な変数の組み合わせになっていることがわかるかと思います。

$H=U+PV$とすることで自然な変数を$S,V$の組から$S,P$に変えることができるということだね。

その通りです。さらに$G=H-TS$とするとさらに自然な変数を$T,P$に変換できるよ。
まとめ
このページではMDから得られている$U(T,V)$と$P(T,V)$から出発して、内部エネルギー$U$とエンタルピー$H$の自然な変数の組み合わせについて考えました。
熱力学関数($U,H,F,G$)における自然な変数は教科書や参考書でよく出てくる話ですが、あまり具体的な数値や変換のイメージが付きにくい分野であります。
MDの数値結果を利用して、少しでも自然な変数の組み合わせについて親しみをもっていただければと思います。











